La tuberculose représente un problème majeur de santé notamment en Afrique subsaharienne, partie du monde la plus touchée. Chaque année, on dénombre environ 9 millions de nouveaux cas de tuberculose et près de 2 millions de personnes en meurent. C’est la huitième grande cause de décès dans les pays à revenu faible et intermédiaire..
Pourtant, la tuberculose est une maladie curable. Son traitement repose sur une chimiothérapie normalisée et une bonne prise en charge des cas. Plusieurs schémas thérapeutiques normalisés sont recommandés selon les différentes catégories, parmi eux le schéma de retraitement. Celui-ci concerne les patients précédemment traités qui ont ensuite des frottis ou des cultures positifs (du fait d’un échec thérapeutique, d’une rechute ou d’un retour après abandon du traitement). Ces patients en schéma de retraitement sont les plus à risque de développer une résistance acquise..
L’avènement de souches de bacilles multirésistants aux antituberculeux majeurs ne vient qu’aggraver l’état d’urgence décrété par l’Organisation Mondiale de la Santé depuis 1993. Vu l’ampleur du problème, des cibles mondiales de réduction de la charge de morbidité de la tuberculose ont été fixées dans le contexte des objectifs du Millénaire pour le développement (OMD) et du Partenariat Halte à la tuberculose. L’Objectif du Plan mondial Stop TB est d’içi 2015 de réduire les taux de prévalence et de mortalité de 50 % par rapport à ce qu’ils étaient en 1990 et d’ici 2050 pour éliminer la tuberculose en tant que problème de santé publique. Cela consiste à atteindre une incidence mondiale de la tuberculose évolutive inférieure à un cas pour un million d’habitants par an. L’une des stratégies repose sur le renforcement du dépistage précoce des cas suspects de tuberculose multi résistante: à savoir tous les cas de retraitement [52].
DEFINITION
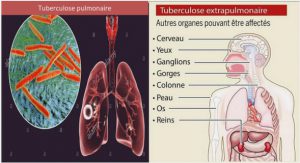
La tuberculose est une maladie infectieuse contagieuse, endémo-épidémique et mal immunisante due aux mycobactéries du complexe tuberculosis regroupant Mycobacterium tuberculosis [bacille de Koch (BK)] et beaucoup plus rarement, Mycobacterium bovis et Mycobacterium africanum. L’atteinte pulmonaire est la plus fréquente mais elle est susceptible d’infecter tous les tissus de l’organisme.
HISTORIQUE
La tuberculose est connue depuis des milliers d’années. Des séquelles de cette maladie ont été décrites sur des momies égyptiennes (1000 ans avant JC) par des médecins archéologues. Les grecs la nommaient « phtisie », c’est à dire consomption, la comparant à un feu intérieur qui brûlait les viscères. Elle était souvent confondue avec bien d’autres affections pulmonaires. C’est seulement aux 18ème et 19ème siècles que des progrès significatifs seront réalisés dans la compréhension et le traitement de cette maladie. Le terme de «tuberculose » va être employé pour la première fois dans son sens actuel par le médecin allemand Johann Lukas SCHÔNLEIN en 1834. René-ThéophileMarie-Hyacinthe LAENNEC affirme son unicité tant sur le plan anatomique que sur le plan clinique. Il l’isole et la distingue des autres affections pulmonaires. En 1882, Robert KOCH découvre le bacille tuberculeux humain: Mycobacterium tuberculosis et réussit sa culture sur sérum de bœuf coagulé en 1884. Il mit au point la tuberculine. En 1909 la tuberculine fut utilisée par Charles MANTOUX (1879-1947). Dès 1924, Albert CALMETTE (1863 1933), et Jean-Marie Camille GUERIN (1872- 1961) mirent au point la vaccination par le BCG (bacille de Calmette et Guérin).
La chimiothérapie antituberculeuse est apparue à la fin de la deuxième guerre mondiale. En effet, jusqu’aux années 1950, les traitements antituberculeux furent lourds et très souvent inefficaces conduisant à la création d’établissements spécialisés (sanatoriums) dont le premier fut ouvert en 1854 en Allemagne. En 1944, Selman Abraham WAKSMAN découvre le premier antibiotique actif contre le bacille tuberculeux : la streptomycine. D’autres médicaments seront découverts dans les vingt années qui ont suivi : l’ethambutol en 1951, l’isoniazide et le pyrazinamide en 1952, l’éthionamide en 1956, la rifampicine en 1969.
EPIDEMIOLOGIE
Situation de la tuberculose dans le monde
En 2011, le nombre de nouveaux cas de tuberculose dans le monde a été estimé à 8,7 millions (fourchette à 125 cas pour 100.000 habitants) [80]. Environ 53 % des cas se trouvent sur le continent asiatique, et 26 % en Afrique. La région sud méditerranéenne enregistre beaucoup moins de cas avec 7,7 % du taux mondial, suivie de l’Europe avec 4.3% et de l’Amérique 3 %.
Parmi les 8,7 millions de nouveaux cas de tuberculose, 0,5 million concerne les enfants et 2,9 millions les femmes. Au niveau mondial, il faut signaler qu’en 2009, près de 10 millions d’enfants ont perdu leurs parents à cause de la tuberculose. Sur les 8,7 millions de nouveaux cas, environ 1,1 millions sont des infectés par le VIH soit 13%. En 2011, 1,4 million de personnes sont mortes de tuberculose (14 décès pour 100.000 habitants). Plus de 95% des décès se sont produits dans les pays à revenu faible et intermédiaire. Chez les personnes vivant avec le VIH, la tuberculose est une cause majeure de décès et est responsable d’un quart de tous les décès. Au niveau mondial, les taux de succès thérapeutiques se sont maintenus à des niveaux élevés pendant plusieurs années.
En 2010 (dernière année pour laquelle les données sur l’issue du traitement sont disponibles), le taux de succès thérapeutique était de 85 % chez les cas nouvellement diagnostiqués et de 87 % chez les cas de tuberculose pulmonaire à frottis positifs (cas les plus contagieux). À l’échelle mondiale, on estime que 3,7 % des nouveaux cas et 20 % des cas traités antérieurement sont porteurs de bacilles multirésistants. Cependant si le nombre de cas de tuberculose multirésistante est en augmentation, on estime que seul un cas sur cinq (19 %) est notifié. L’Inde, la Chine, la Fédération de Russie et l’Afrique du Sud totalisent près de 60 % des cas de tuberculose multirésistante. C’est en Europe de l’Est et en Asie centrale, que l’on relève les plus fortes proportions de cas de tuberculose multirésistante.
FORMES CLINIQUES
Type de description : Tuberculose pulmonaire commune chez le sujet immunocompétent
Signes fonctionnels
Ils sont polymorphes et comprennent :
• Une toux sèche au début, tenace, à recrudescence matinale, mais sans horaire précis, productive par la suite ramenant une expectoration muqueuse au début puis légèrement purulente. D’ abord d’horaire matinal puis sans horaire précis, elle peut être hémoptoïque ou accompagnée d’une hémoptysie sévère.
• Des douleurs thoraciques rythmées par la respiration et la toux.
• Une dyspnée qui se manifeste d’abord à l’effort, ensuite au repos.
• Une hémoptysie
• Une dysphonie et des troubles de la déglutition peuvent parfois être associés au tableau.
Signes généraux
Ils associent de manière variable :
• une asthénie physique et psychique qui ne cède pas au repos. Elle s’accentue en fin de journée et reste tenace.
• un amaigrissement parfois, rapide ou important.
• une anorexie non sélective.
• une fièvre vespéro-nocturne irrégulière, bien tolérée, s’accompagnant de sudation profuse à prédominance nocturne.
Signes physiques
L’examen physique retrouve:
• des râles crépitants isolés ou dans le cadre d’un syndrome de condensation pulmonaire complet.
• parfois l’examen clinique peut être normal.
Signes paracliniques
Eléments d’orientation
• L’hémogramme
Il peut mettre en évidence un syndrome inflammatoire biologique : une anémie, une CRP élevée ou une VS accélérée.
• L’intradermoréaction à la tuberculine (IDR)
Il consiste à injecter un dixième de millilitres de tuberculine dans le derme à la face antérieure de l’avant- bras (voir figure 4). Un aspect de peau d’orange atteste de la bonne pratique de l’injection. La lecture de l’IDR se fait à la 72ème heure. La réaction est positive si la taille de l’induration est supérieure à huit millimètres. Toutefois l’IDR peut être négative en cas de mauvaise technique d’injection ; d’injection au cours de la période anté-allergique ; de déficit immunitaire ; ou de retard de réaction.
• Radiologie
Les radiographies du thorax de face et profil peuvent révéler deux sortes d’images élémentaires :
– la caverne : qui est une clarté arrondie ou ovalaire siégeant au sein d’un infiltrat à limites internes nettes. Parfois on observe une image hydro-aérique avec une bronche de drainage souvent visualisée sous forme d’ « image en rail » allant vers l’hile. Toutes les topographies sont possibles, mais l’atteinte des segments apicaux et dorsaux est plus fréquente .
– le nodule : qui est une opacité arrondie, dense assez homogène, de contours flous de taille variant du « grain de mil » au micro ou macronodules. La confluence est fréquente et réalise une image d’infiltrat matérialisée par une opacité inhomogène non systématisé et mal délimitée.
Eléments de certitude
La bactériologie
• La Bacilloscopie : confirme la présence de bacilles acido alcoolo résistant (BAAR) dans les expectorations. Elle est effectuée sur des crachats du matin collectés durant trois jours consécutifs. Les produits recueillis seront examinés au microscope après coloration au Ziehl-Neelsen ou coloration fluorescente à l’auramine-rhodamine.
• La culture après décontamination, fluidification, homogénéisation puis ensemencement sur milieu de Lowenstein-Jensen, permet de préciser la nature des mycobactéries. Deux méthodes beaucoup plus délicates et plus coûteuses sont utilisées dans certains laboratoires pour pallier la lenteur de croissance du bacille de Koch.
La culture sur milieu gélosé (milieu de Middlebrook) : les cultures sont examinées à la loupe binoculaire après 3 à 4 semaines (au lieu de 4 à 6 par la méthode classique). La culture sur milieu liquide : les cultures sur des milieux liquides, soit radioactif (Système Bactec), soit non radioactif (MGIT : Middlebrook, Mycobacteria Growth Indicator Tube) permettent de détecter les bacilles en 8 à 14 jours.
• L’antibiogramme fait avec les antibiotiques majeurs (isoniazide, rifampicine, streptomycine, pyrazinamide) permet la détection de résistance.
L’anatomopathologie
L’examen histologique des pièces de biopsie (pleurale, ganglionnaire, cutanée…etc.) retrouve un granulome épithélioïde gigantocellulaire qui est un amas de cellules claires (macrophages) à noyau ovalaire réniforme et à cytoplasme clair (le nom « épithélioïde » provient de la forme du noyau). Ces cellules épithélioïdes peuvent fusionner pour donner des cellules multinucléées géantes appelées cellules de Langhans ; puis il se produit un agencement des noyaux en couronne à la périphérie du cytoplasme. Tout autour de ces amas macrophagiques il existe beaucoup de lymphocytes: LT actifs.
|
Table des matières
INTRODUCTION
PREMIERE PARTIE : RAPPELS
1. DEFINITION
2. HISTORIQUE
3. EPIDEMIOLOGIE
4. PATHOGENIE
5. FORMES CLINIQUES
5.1. Type de description : Tuberculose pulmonaire commune chez le sujet immunocompétent
5.2. Autres formes cliniques
5.2.1. La miliaire tuberculeuse
5.2.2. La tuberculose des séreuses
5.2.3. La tuberculose ganglionnaire
5.2.4. Tuberculose ostéo-articulaire
5.2.5. Méningite tuberculeuse
5.2.6. Tuberculose viscérale
5.2.7. Tuberculose multifocale
5.2.8. Formes selon le terrain
6. TRAITEMENT
6.1. Traitement curatif
6.1.1. Buts
6.1.2. Moyens
6.1.2.1. Les antituberculeux de première intention
6.1.2.2. Les antituberculeux de seconde intention
6.1.2.3. Moyens adjuvants
6.1.2.4. Conduite du traitement
6.1.3. Indications
6.1.3.1. Les nouveaux cas
6.1.3.2. Le retraitement
6.1.3.3. Cas particuliers
6.1.4. Surveillance du traitement
6.2. Traitement préventif
6.2.1. Prévention primaire
6.2.1.1. Information- Education-Communication (IEC)
6.2.1.2. Dépistage et prise en charge des cas
6.2.1.3. La vaccination
6.2.2. Prévention secondaire
6.2.2.1. La chimioprophylaxie à l’isoniazide
6.2.2.2. Isolement des sujets contacts
DEUXIEME PARTIE : TRAVAIL PERSONNEL
1. CADRE D’ETUDE
2. PATIENTS ET METHODES
2.1. Type d’étude
2.2. Population d’étude
2.3. Recueil des données
2.4. Saisie et exploitation des données
3. RESULTATS
3.1. Résultats descriptifs
3.1.1. Aspects épidémiologiques
3.1.1.1. Répartition de la population d’étude en fonction du sexe
3.1.1.2. Répartition de la population d’étude selon les tranches d’âge
3.1.1.3. Répartition de la population d’étude en fonction le niveau de scolarisation
3.1.1.4. Répartition de la population d’étude selon la profession
3.1.1.5. Répartition de la population d’étude selon le mode de vie
3.1.1.6. Répartition de la population en fonction de la notion de contage tuberculeux
3.1.2. Aspects cliniques
3.1.2.1. Répartition de la population en fonction de la durée d’évolution des symptômes
3.1.2.2. Répartition de la population en fonction des signes cliniques
3.1.2.3. Répartition de la population d’étude en fonction de la localisation de la tuberculose
3.1.3. Aspects paracliniques
3.1.3.1. Répartition de la population d’étude selon le statut sérologique
3.1.3.2. Répartition de la population d’étude selon le profil sérologique
3.1.3.3. Répartition de la population en fonction du taux de lymphocytes TCD4
3.1.3.4. Répartition de la population d’étude en fonction de la bacilloscopie
3.1.3.5. Répartition de la population en fonction des résultats de culture des crachats
3.1.3.6. Répartition de la population d’étude en fonction des résultats d’antibiogramme
3.1.4. Aspects thérapeutiques
3.1.4.1. Délai de mise sous retraitement
3.1.4.2. Répartition de la population d’étude en fonction des circonstances de mise sous protocole de retraitement
3.1.5. Aspects évolutifs
3.1.5.1. Répartition de la population d’étude en fonction des résultats des contrôles de recherche de BAAR
3.1.5.2. Répartition de la population d’étude en fonction des résultats du retraitement
3.2. Résultats analytiques
3.2.1. Répartition de la population d’étude en fonction du sexe et de l’âge
3.2.2. Répartition de la population d’étude en fonction des circonstances et des résultats du retraitement
3.2.3. Répartition de la population d’étude en fonction du statut sérologique et des circonstances de retraitement de tuberculose
3.2.4. Répartition de la population d’étude en fonction du statut sérologique et l’issue du retraitement
4. DISCUSSION
4.1. Aspects épidémiologiques
4.1.1. L’âge
4.1.2. Le sexe
4.1.3. Le niveau de scolarisation et la profession
4.1.4. Mode de vie
4.2. Aspects cliniques et paracliniques
4.2.1. Les signes cliniques et la localisation
4.2.2. Recherche de BAAR
4.2.3. Culture des expectorations et antibiogrammes
4.2.4. Le statut et profil sérologiques
4.2.5. Les taux de CD4
4.3. Aspects thérapeutiques
4.3.1. Les circonstances de retraitement
4.3.2. Délai de retraitement
4.4. Aspects évolutifs
4.4.1. Contrôles de recherche des BAAR
4.4.2. Résultats du retraitement
CONCLUSION