Télécharger le fichier pdf d’un mémoire de fin d’études
MATIERES PREMIERES
Une formulation optimale de boissons rafraîchissantes doit inclure à part l’eau, un produit sucrant (sucre ou édulcorant de synthèse), des acides, des arômes et éventuellement du dioxyde de carbone. D’autres ingrédients tels que des colorants, du caramel, des extraits de plante et de la caféine peuvent entrer dans leur composition. Nous détaillerons les principaux constituants tels que le sucre, les additifs et le CO2 [4].
Le saccharose
Le saccharose a pour rôle principal d’apporter à une boisson rafraichissante, une saveur sucrée équilibrée, du corps (viscosité en bouche), de jouer le rôle d’exhausteur d’arômes, d’équilibrer entre elles les différentes qualités organoleptiques (acidité, aromes, flaveur) pour une meilleure appréciation par le consommateur. Les limonadiers ont établi des spécifications précises pour une qualité de sucre que les sucriers s’efforcent de satisfaire. [5]
Les additifs
Un additif alimentaire est défini comme «n’importe quelle substance habituellement non consommée comme un aliment en soi et non employée comme un ingrédient caractéristique de l’aliment, qu’il ait une valeur nutritionnelle ou non, dont l’addition intentionnelle à l’aliment pour un but technologique dans la fabrication, le traitement, la préparation, l’emballage, le transport ou le stockage devient, ou peu s’attendre raisonnablement à devenir, lui ou l’un de ses dérivés, directement ou indirectement, un composant de cet aliment » (directive 89/107/EEC). [6]
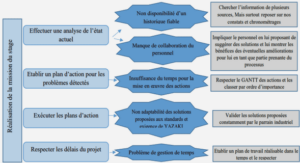
En bref, et plus simplement, un additif alimentaire est une substance ajoutée intentionnellement aux denrées alimentaires pour remplir certaines fonctions technologiques, comme colorer, sucrer ou conserver. La nomenclature distingue plusieurs classes d’additifs selon leurs effets technologiques sur l’aliment. La figure 1 comporte la liste des principaux types d’additifs alimentaires :
La plupart des additifs ne peuvent être utilisés que dans certaines denrées alimentaires et en quantité limitée. L’utilisation des additifs alimentaires doit toujours être mentionnée sur l’emballage des produits alimentaires ainsi que leur catégorie (conservateur, antioxydant, …) avec leur nom ou leur numéro E.
Quelques additifs échappent à la législation de l’étiquetage (en boulangerie, en pâtisserie, le vin et aussi les solvants qui permettent l’extraction de certains colorants végétaux ou de fruits [5].
Les acidifiants
Parmi les critères de qualité de boissons rafraichissantes, l’équilibre sucré/ acide est essentiel. En choisissant un acide, on doit veiller à ce qu’il ait un profil intensité/ comparable à celui du produit sucrant. Les acides citrique (E330) et malique (E 296) qu’on utilise habituellement n’ont pas le même profil. L’acide citrique a une saveur pure forte mais qui disparait rapidement. Elle s’harmonise bien avec le saccharose dont la saveur sucrée disparait rapidement. Pour les édulcorants artificiels qui ont une persistance plus longue que le sucre, il vaut mieux utiliser l’acide malique dont la saveur acide est persistante. Avec les mélanges Aspartame/ Acesulfame K, l’utilisation donne un bon équilibre acide/sucré [5].
Les édulcorants
Il est difficile de remplacer les sucres sans altérer la qualité de la saveur d’une boisson rafraichissante. Ainsi l’équilibre des saveurs sucrées/ acide devient citrique en remplaçant le sucre par les édulcorants dans les boissons dites Light. On est amené à utiliser un sel d’acide citrique pour tamponner le milieu. Suivant l’édulcorant utilisé, le rapport citrate/acide citrique est modifié. Avant 1883, les boissons allégées utilisaient surtout la saccharine (E 954). Aujourd’hui c’est l’aspartame (E) et les mélanges Acesulfame/Aspartame qui sont les plus fréquemment employés. Les avantages de l’utilisation de ce mélange sont la qualité de saveur, la synergie avec les produits sucrant de masse et le prix de revient [5].
Les arômes
Les boissons rafraichissantes sont un domaine d’innovation permanente en matière d’aromatisation. Les notes aromatiques les plus fréquentes sont à base de fruit (citron, orange (E 110), pêche, citron vert, jaune (E 102 Tartrazine)). On utilise également des extraits de plante, d’épices mais aussi du caramel (E 150) et du miel [5].
Les conservateurs
Est appelé conservateur toute substance capable de s’opposer aux altérations d’origines chimiques ou microbiologiques. Les conservateurs sont réglementés sous forme de listes positives et négatives. L’intégration d’un conservateur dans une liste et la détermination du seuil maximal d’utilisation se font selon deux critères principaux :
l’intérêt technologique du conservateur ;
les interactions et impacts avec l’environnement proche (échanges contenus-contenant, impact sur la santé du consommateur et sur l’environnement en général). Les altérations peuvent être soit chimiques soit biologiques. Ils sont utilisés pour « lutter » contre les différents types d’altérations :
chimiques : antioxydants, anti-UV, anti ozonant, retardateur de flamme,…
biologiques : antifongiques, antibactériens,…
Certains additifs de conservation peuvent jouer le double rôle d’antimicrobien et d’anti oxygène.
Les substances utilisées peuvent être organiques (acides carboxyliques) ou minérales (nitrates, sulfites ou sels). Quelle que soit leur nature, les conservateurs doivent figurer sous le nom « conservateur » suivi de leur nom ou de leur numéro d’identification conventionnel (E 2XX). Le plus utilisé est l’acide benzoïque (E 210) obtenu soit par extraction de baies, soit par synthèse. Il est également disponible sous trois formes de sels : benzoate de sodium (E 211), benzoate de potassium (E 212), benzoate de calcium (E 213). Il est actif sous forme non ionisé à pH<4, inhibant des bactéries. Comme les sels sont très solubles dans l’eau (au contraire de l’acide), ils sont principalement employés.
Pouvant présenter quelques problèmes de toxicité, la dose maximale est de 150 mg/L, exprimée en acide benzoïque [5]
Les émulsifiants
Ce sont des agents de texture que l’on retrouve sur l’emballage des produits alimentaires. Ils donnent le volume, la tenue ou le moelleux aux produits. D’une manière générale, ils sont moins toxiques que les colorants, conservateurs ou antioxydants [5].
Le dioxyde de carbone
Les boissons carbonatées contiennent du CO2 dans les limites de solubilité de ce gaz en fonction de la pression de gazéification généralement de 3-4 bars.
L’utilisation d’édulcorants artificiels peut modifier la qualité des bulles de CO2 qui deviennent plus grosses et provoquent un phénomène de moussage intempestif [5].
FABRICATION
Les boissons rafraichissantes sucrées sont essentiellement fabriquées par des opérations de mélange et de stabilisation par la chaleur avant conditionnement aseptique. Suivant le type de boisson, la composition, la viscosité, l’acidité,… on procédera à des traitements thermiques de stabilisation différents. Ainsi, le choix de la méthode de traitement repose sur les critères suivants :
Type de produit (jus, nectar, boissons carbonatée ou non) ;
Acidité du produit traité et rapport Brix/acide (il est connu que les germes acidophiles sont moins thermophiles et nécessitent des températures de pasteurisations plus basses) ;
Présence de pulpes de fruits qui augmentent la viscosité et modifient les propriétés rhétoriques du produit ;
Durée de vie du produit désiré et qui dépend de la composition du produit, du barème de pasteurisation, de la nature de l’emballage et de la température de distribution ;
Eventuellement, désaération et homogénéisation. La désaération vise à éviter l’oxydation de la vitamine C pendant le stockage. On la pratique plus en cas de remplissage à froid qu’en remplissage à chaud [5].
QUALITE DES BOISSONS RAFRAICHISSANTES
La saveur sucrée est le paramètre essentiel dans l’estimation de la qualité du goût des boissons sucrées. C’est pourquoi on utilise des densimètres de précision pour contrôler le sucre dans ces produits. Pour les boissons allégées, on a recours à l’analyse objective au laboratoire (pH, acidité titrable, réfractomètre, polarimètre, HPLC pour les édulcorants, densité) et à l’évaluation sensorielle par un jury. Etant donnés, la très forte sucrosité des édulcorants artificiels et leurs défauts tels que l’arrière-goût amer et métallique et la persistance de leurs saveurs, une très faible variation du dosage peut entraîner une qualité de saveur et un équilibre sucré/acide défectueux. On retrouve parfois dans les mélanges de sucres et deux ou plusieurs édulcorants artificiels une qualité proche de celle du saccharose. Il est enfin un constituant essentiel et majoritaire à ne pas oublier, c’est l’eau, dont la qualité est déterminante dans la qualité des boissons gazeuses. Elle intervient par son goût, son pH, son alcalinité, son acidité, sa teneur en azote et matières organiques ainsi que sa qualité bactériologique. Elle subit généralement des traitements pour répondre aux normes requises dans les boissons [5].
GENERALITES SUR L’INDICE DE REFRACTION
L’INDICE DE REFRACTION
DEFINITION ET CARACTERISTIQUES
Définition
C’est la propriété d’un milieu transparent caractérisant la propagation de la lumière et des ondes électromagnétiques. Numériquement, il correspond au rapport de la vitesse de la lumière dans le vide (C) à celle dans un milieu matériel (V). n C , (C = 3.108 ms-1)
Dans un milieu différent, transparent, la vitesse de propagation V est toujours inferieure à C (V<C). Si le milieu est isotrope, cette vitesse est indépendante de la direction. Sa valeur est supérieure ou égal à 1 et n’a pas de dimension [7]. On appelle réfraction le changement de direction que subit la lumière lorsqu’elle traverse la surface de séparation de deux milieux transparents (figure 2).
Cette réfraction est régie par les lois de Snell-Descartes :
Première loi ; Le rayon incident SI, le rayon réfracté IR et la normale au point d’incidence NIN’ sont dans le même plan (plan d’incidence) ;
Deuxième loi ; soient i1 et n1 l’angle d’incidence et l’indice de réfraction du premier milieu (milieu par lequel arrive la lumière), i2 et n2 l’angle d’incidence et l’indice de réfraction du second. On aura alors : n1 sin i1 n2 sin i2
Si l’indice du second milieu est plus élevé que celui du premier (passer de l’air à l’eau), on dit que le second milieu est plus réfringent que le premier (n2 > n1). n1 sin i1 n2 sin i2
On aura alors sini1 > sini2, i1 > i2. Le rayon réfracté est plus proche de la normale que le rayon incident. En augmentant i1 jusqu’à sa valeur maximale sensiblement égale à 90°, i2 prend sa valeur maximale l telle que : n1 sin 90 n2 sin n sin 14.
Les réfractomètres
Le réfractomètre d’Abbe (figure 4)
Le réfractomètre d’Abbe permet d’avoir une mesure de l’indice de réfraction d’un liquide en le déposant sur une surface en verre, en l’enfermant dans un dispositif optique, et en réglant un bouton pour amener une plage éclairée au centre d’un réticule [7].
Ce réfractomètre a été décrit, en 1874, par son inventeur, Ernst Abbe. Dans son étude sur les réfractomètres de 1901, Culmman décrit cet instrument comme constitué de deux prismes en verre flint enfermant une mince couche de 1/20e de millimètre d’épaisseur du liquide à examiner. Le prisme inférieur sert surtout à maintenir le liquide et à permettre l’éclairage du prisme supérieur. Dans les réfractomètres modernes, le prisme supérieur sert à l’éclairage et le prisme inférieur est celui qui permet la mesure.
Le principe consiste à éclairer le liquide à analyser en lumière rasante et à déterminer l’angle limite noté e qui dépend de l’indice n cherché et de l’indice N du matériau sur lequel repose le liquide et dans lequel le rayon rasant rentre.
N = N sin e Ce rayon poursuit son chemin et attaque la face de sortie du prisme avec l’angle : r = α – e où α est l’angle du prisme. Le rayon sort donc du prisme avec l’angle i tel que : N sin r = sin i
L’angle i est en relation avec l’indice recherché n. Un viseur pointe l’angle et est gradué directement en indice de réfraction. La valeur est précise à deux unités de la quatrième décimale de la valeur de l’indice n. Comme il n’est pas possible d’avoir un unique rayon rasant qui rentre au bon endroit dans le support matériel sous-jacent, le dispositif met en jeu un faisceau de lumière dont la limite est, par construction, le rayon rasant. Ce faisceau constitue la plage de lumière dont la limite sera ajustée au réticule et sera la base de la mesure. La figure ci-dessous représente ce dispositif. Le prisme supérieur est éclairé et contient le rayon rasant. La lumière entre dans le prisme inférieur en une plage de lumière dont le rayon supérieur correspond au prolongement du rayon rasant.
À la sortie du prisme, cette plage de lumière est réfléchie par un miroir et est observée par une lunette collimatrice. L’utilisateur peut observer, dans cette lunette, la plage de lumière et sa limite qui porte l’information sur l’angle limite, donc sur l’indice de réfraction du liquide étudié (figure 5) [7].
Le réfractomètre universel (type OPL)
A l’avant est fixé le prisme de référence sur lequel s’articule un prisme d’éclairage ou prisme auxiliaire. Quand ce prisme est rabattu, les montures des deux prismes forment un compartiment de faible épaisseur destiné à recevoir les liquides, et la lumière est admise par la fenêtre antérieure. La rotation du miroir permet d’amener le rayon limite parallèle à l’axe de la lunette ; on le vérifie en pointant dans la lunette (1) la limite de séparation entre la zone claire et la zone obscure. Le miroir entraine dans sa rotation un secteur gravé, dont on lit à l’oculaire (2), l’échelle graduée en indice. Un prisme compensateur tournant autour de l’axe de visée permet de supprimer les colorations que présente la limite de séparation lorsqu’on utilise une lumière blanche (figure 6).
Pour les solutions de saccharose, l’échelle est graduée en outre, en pourcentage de saccharose dans la solution. L’indice d’une substance dépendant beaucoup de la température. Les prismes comportent un ensemble thermostaté permettant d’obtenir une température constante
Les réfractomètres différentiels
Ces appareils utilisent la détermination de la déviation d’un faisceau de lumière. On considère un faisceau de lumière monochromatique, traversant une lame à faces parallèles, formée de deux prismes creux, contenant deux liquides. Lorsque ces deux liquides sont identiques, le faisceau n’est pas dévié et converge au point O (figure 7 a et b). Lorsque les deux prismes creux sont remplis de liquides différents, (fig.7 b), les rayons subissent une déviation, à la traversée de l’interface AB. Ils convergent alors, dans le plan focal de l’objectif O2, en un point M différent de O. la déviation, d= OM, dépend de la différence entre les indices n1, n2, des deux liquides (1) et (2). Si un des liquides a un indice parfaitement déterminé, on peut ainsi déduire l’indice de l’autre. Il est important que l’ensemble des deux prismes soit à la même température, ce qui nécessite un dispositif thermostaté.
Les réfractomètres différentiels automatiques
Le principe de la réfractométrie différentielle est appliqué à la détection, en chromatographie liquide (HPLC). Le refractomètre différentiel analyse, alors, en permanence, la différence d’indice entre la phase mobile contenue dans le prisme de référence (ou cellule de référence), et la phase mobile, qui élue la colonne, contenue dans l’autre prisme (ou cellule de mesure).Lorsque les prismes contiennent le même liquide, un dispositif de réglage de zéro permet aux cellules photoélectriques de délivrer un signal identique. Lorsque l’échantillon est différent du liquide de référence, le faisceau lumineux subit une déviation et l’une des deux cellules photoélectriques est moins éclairée. La différence entre les signaux délivrés par chaque cellule photoélectrique est amplifiée et commande la plume d’un enregistreur (figure 8) [7].
Le rapport de stage ou le pfe est un document d’analyse, de synthèse et d’évaluation de votre apprentissage, c’est pour cela chatpfe.com propose le téléchargement des modèles complet de projet de fin d’étude, rapport de stage, mémoire, pfe, thèse, pour connaître la méthodologie à avoir et savoir comment construire les parties d’un projet de fin d’étude.
|
Table des matières
Introduction
Première partie : Généralités sur les boissons gazeuses et l’indice de réfraction
CHAPITRE I : GENERALITES SUR LES BOISSONS GAZEUSES
I. DEFINITION
II. HISTORIQUE
III. MATIERES PREMIERES
1. Le saccharose
2. Les additifs
2.1 Les acidifiants
2.2 Les édulcorants
2.3 Les arômes
2.4 Les conservateurs
2.5 Les émulsifiants
3. Le dioxyde de carbone
IV. FABRICATION
V. QUALITE DES BOISSONS RAFRAICHISSANTES
CHAPITRE II : GENERALITES SUR L’INDICE DE REFRACTION
I. L’INDICE DE REFRACTION
1. DEFINITION ET CARACTERISTIQUES
1.1 Définition
1.2 Caractéristiques
a La température
b La pression
c La longueur d’onde
d Cas des solutions
II. MESURE DE L’INDICE DE REFRACTION
1. . Généralités
2. Les réfractomètres
2.2 Le réfractomètre universel (type OPL)
2.3 Les réfractomètres différentiels
2.4 Les réfractomètres différentiels automatiques
3. APPLICATIONS
3.1 La réfractométrie simple
3.2 la réfractométrie différentielle
Deuxième partie : Travail expérimental
CHAPITRE I : MATERIEL ET METHODE
I. CADRE DE L’ETUDE
II. MATERIEL
1. Echantillons
2. Appareillage et verrerie
III. METHODE
1. Vérification des données sur l’emballage
2. Préparation des solutions étalon de saccharose
3. Le réfractomètre type Atago T2
3.1 Principe
3.2 Mode opératoire
CHAPITRE II : RESULTATS
I. DONNEES MENTIONNEES SUR LES EMBALLAGES
II. MESURE DE L’INDICE DE REFRACTION
1. Avec les solutions étalons
2. Avec les échantillons de boissons gazeuses
3. Comparaison des valeurs obtenues avec le réfractomètre avec celles obtenues sur le territoire français (métropole et outre-mer)
CHAPITRE III : DISCUSSION
Conclusion
REFERENCES BIBLIOGRAPHIQUES
Télécharger le rapport complet