Télécharger le fichier pdf d’un mémoire de fin d’études
Morphologie et structure de Helicobacter pylori :
La morphologie de Helicobacter pylori:
Helicobacter pylori est une bactérie à gram négatif.
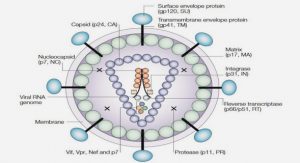
Elle a une forme en virgule ou en S, qui correspond à une forme spiralée dans l’espace mesurant 2,5 à 4 μm de long et 0,5 à 1μm d’épaisseur (Figure.1).
Elle porte 4 à 6 flagelles permettant à la bactérie de se glisser à travers les muqueuses de l’estomac et s’ancre aux cellules épithéliales et qui sont entourées d’une gaine résistible à l’acide. [32, 35, 36, 86, 87 ]
A l’extrémité distale de ses flagelles, à la différence des autres espèces de Campylobacter, on observe un bulbe ou disque [60,62]. Le reste de la surface de H.pylori est lisse.
La structure chimique de Helicobacter pylori:
La structure protéique:
La structure protéique de la cellule entière, de la membrane externe, de l’extrait acide de la surface protéique, et du lysat cellulaire, a été étudiée par électrophorèse sur gel de polyacrylamide en présence de dodecyl sulfate de sodium [103].
La structure de la paroi cellulaire:
La paroi cellulaire de Helicobacter pylori est riche en acides gras [50].
Le génome [82]:
Les données génomiques ont incontestablement confirmé le rôle de la mobilité dans le pouvoir de la colonisation de la muqueuse gastrique ; au delà des gènes préalablement connus tels que les gènes flaA [55], flaB [56], flbA [57], flbE [58] codant respectivement pour les flagellines majeures et mineures, un modulateur, et le crochet d’ancrage du flagelle.
Une vingtaine d’autres gènes ont été identifiés qui codent pour des homologues de la machinerie d’assemblage et de sécrétion des flagellines présents chez d’autres bactéries.
23% des protéines prédites de H.pylori n’ont pas d’homologues connus actuel-lement dans le monde du vivant, et sont codées par des gènes dits <<orphelins >>, une donnée qui est toute relative et qui peut être amenée à changer au fur et à mesure de la publication de nouveaux génomes. De tels gènes apparaissent comme des candidats d’intérêt majeur car à priori spécifiques de H.pylori.
Le profil génomique est déterminé à l’aide d’une technique rapide d’extraction de l’ADN chromosomique de H.pylori, et l’analyse par des techniques de restriction.
Biologie de Helicobacter pylori :
Ecologie :
Le pH :
Helicobacter pylori survit dans le lumen de l’estomac à un pH très acide situé entre 1 et 4 grâce à son activité uréasique très importante, il entraîne une libération d’ammoniac à partir de l’urée, ce qui lui permet d’augmenter le pH à son contact, et qui a pour effet immédiat de neutraliser l’environnement à la proximité de la bactérie ce qui expliquerait sa résistance à l’acidité de l’estomac [24,94].
Toutes les souches isolées en clinique produisent une uréase en quantité abondante (près de 6 % des protéines totales). L’uréase est un métalloenzyme multimérique à ion nickel [141] (Figure.2). Pour être catalytiquement active, l’uréase requiert l’expression de deux sous unités structurales (Ure A, Ure B) et de quatre protéines dites auxiliaires (Ure E, Ure F, Ure G et Ure H) qui permettent l’activation de l’uréase en enzyme fonctionnelle par incorporation des ions nickel aux sites actifs du complexe enzymatique. Une autre protéine dite Ure I coexprimée avec les protéines auxiliaires n’est pas nécessaire à la synthèse d’une uréase active. Cependant elle joue un rôle prépondérant dans la résistance à l’acidité et elle est essentielle à la colonisation de la muqueuse gastrique murine par H.pylori [34].
Conditions respiratoires :
H.pylori est dite micro aérophile, c’est-à-dire qu’elle nécessite un apport d’oxygène, mais dans des proportions inférieures à celles trouvées dans l’atmosphère [87].
H.pylori exige une atmosphère renferment : 5% d’O2, 10% de CO2, 85% de N (azote) [87].
Conditions de température :
La croissance de H.pylori se fait dans des degrés de températures situés entre 35°et 37°C.
Le mode nutritionnel :
H.pylori tire son énergie de certains acides aminés, ou certains intermédiaires du cycle des acides tricarboxyliques : glutamate, aspartate, serine. Cette énergie n’est jamais fournie par les hydrates de carbone [32].
Elle a une capacité particulière à capter le fer. En effet, il existe à sa surface des récepteurs qui vont fixer la lactoferrine ou la transferrine et permettre l’acquisition de fer directement de ces protéines [87, 32,35].
La mobilité de Helicobacter pylori :
La mobilité est conférée par la morphologie spiralée de la bactérie ainsi que par la présence de 4 à 6 flagelles unipolaires.
Cette mobilité permet à H.pylori d’échapper rapidement à l’acidité de la lumière gastrique et de pénétrer la souche épaisse du mucus pour atteindre la surface de l’épithélium gastrique où le pH est voisin de la neutralité.
Les filaments flagellaires sont constitués de deux flagellines, la flagélline majeure Fla A et la flagélline mineure Fla B qui sont indispensable à H.pylori pour coloniser durablement la muqueuse gastrique [69].
pathogénie de Helicobacter pylori :
H.pylori a la capacité d’induire une réaction inflammatoire chez l’homme (Figure.3).
Les propriétés de H.pylori permettant l’infection sont maintenant divisées en facteurs de colonisation et en facteurs de pathogénicité :
les facteurs de colonisation :
Ils comprennent la production de l’uréase par H.pylori, la mobilité, la micro-aérobie et les facteurs d’attachement comme les récepteurs bactériens. En effet, EVANS et COLL. [30] ont démontré l’existence d’antigènes bactériens désignés adhésines, capables d’interagir spécifiquement avec des récepteurs cellulaires de l’épithélium gastrique. Ce qui explique que H.pylori ne soit retrouvé qu’en association avec les cellules épithéliales gastriques.
Une fois H.pylori dans l’estomac, son uréase lui serre à produire de l’ammoniaque qui va tomponner le microenvironnement autour de la bactérie [4].
La morphologie et les flagelles de H.pylori lui permettent ensuite de se déplacer dans le mucus et des adhésines qui sont des glycoprotéines lui permettent d’adhérer aux cellules sur un récepteur cellulaire de nature glycolipidique ou autre [91].
Deux types d’adhésines ont été caractérisées génétiquement et biochimiquement:
Une adhésine Bab A2 impliquée dans l’interaction avec l’antigène du groupe sanguin Lewis b exprimé à la surface des cellules gastriques [58].
Deux adhésines homologues Alpha A et Alpha B produites par tous les isolats de H. pylori et permettant à la bactérie d’interagir avec les tissus gastriques [101].
Trois de récepteurs ont été identifiés [33, 70, 95] :
Une structure fimbrillae capable de s’associer à un récepteur de type N-acétyl-lactose non spécifique de l’estomac.
Une <<exo enzyme S >> capable de s’associer au glicocérolipide de type phosphatidyl éthanolamine.
Un matériel superficiel capable d’adhérer aux lignées cellulaires de type Hela.
Les facteurs de pathogénicité de Helicobacter pylori :
Ces facteurs ne sont pas encore bien élucidés. Mais on sait maintenant qu’au niveau de la cellule épithéliale, l’ammoniaque libérée par la réaction de l’urée stomacale avec l’uréase de H.pylori au contact des cellules peut être cytotoxique [53].
De même, la lysocithine et l’alcool déshydrogénase sont produites par l’hydrolyse de la lécithine des membranes cellulaires à l’aide de la phospholipase de l’H.pylori . Et en présence de l’éthanol, il y a production de l’acétaldéhyde . Tous ces métabolites sont cytotoxiques. [79, 3]
Il existe d’autres facteurs de pathogénicité et qui font l’objet de plusieurs études actuellement. Trois protéines, VacA, HP-NAP et CagA ont ainsi caractérisées [39].
La protéine VacA :
La protéine VacA, une cytotoxine vacuolisante active, est produite dans 50% à 65% des souches de H.pylori, codée par un gène de H.pylori et qui serait capable d’induire une vacuolisation des cellules épithéliales in vitro et in vivo chez l’homme, par la formation des pores dans la membrane cellulaire [39].
Une équipe japonaise, a montré comment VacA agit. Elle a d’abord découvert que VacA se fixait à la surface des cellules en s’accrochant à Ptprz, une protéine que l’on croyait jusqu’à maintenant présente exclusivement dans le cerveau et qui assure notamment la cohésion des cellules nerveuses entre-elles. Or les japonais l’ont
repérée et clairement identifiée dans les tissus gastriques et ils ont montré qu’elle se liait spécifiquement à VacA. Le tandem VacA/ Ptprz joue-t-il pour autant un rôle dans l’ulcère ? Seule une souris knock –out, dont on a supprimé un gène dont on souhaite connaître les effets –ici le gène codant pour la protéine Ptprz– pouvait leur en apporter la preuve. C’est ce qu’ils ont fait, Ptprz participe bien au déclenchement de l’ulcère puisque les souris mutées qui n’ont pas Ptprz sont totalement résistantes à la toxine VacA et à l’infection par Helicobacter pylori, ce qui n’est pas le cas des souris non mutées dont l’épithélium se désagrège laissant à nu la muqueuse profonde de l’estomac. En fait, en se fixant à Ptprz, VacA déstabilise cette dernière et provoque la désolidarisation des cellules protectrices de la muqueuse [38].
La protéine HP-NAP :
La protéine HP-NAP se lie à des récepteurs spécifiques de la membrane et par conséquent la stimulation des neutrophiles humains : génération, chimiotactisme et adhésion [28,113].
La protéine CagA :
La protéine CagA (cytotoxin-associated genes A), de masse moléculaire 128 KDa, est exprimée dans 60% à 70% des souches de H.pylori selon les zones géographiques. La présence de cette protéine est corrélée à l’évolutivité de la gastrite et à l’atrophie gastrique [68,105]. En effet une étude française a montré que cette protéine expression du gène cag A est associée à des lésions histologiques plus sévère [8]. Ces résultats confirment les travaux ayant décrit in vitro le rôle de Cag A dans le déclenchement de la réponse inflammatoire [71].
H.pylori agit également sur le mucus qui devient épais et moins hydrophobe, les antigènes diffusibles de Helicobacter pylori vont avoir sur le chimiotactisme et l’activation des monocytes et macrophages induisant une inflammation [91].
Les réactions immunitaires et locales que provoque
Helicobacter pylori :
La colonisation de l’estomac par la bactérie peut stimuler une réponse immunitaire de l’hôte (l’homme) et peut causer des réactions générales et neutrophiliques et la production des anticorps anti- Helicobacter pylori.
Induction de l’inflammation :
La gastrite histologiquement mise en évidence est sans doute une conséquence de la réponse immunitaire locale de l’hôte à l’infection et implique une infiltration de lymphocytes (B et T), cellules plasmatiques, histiocytes et fréquemment des cellules polymorphonucléaires [122].
Une large proportion des cellules lymphoïdes infiltrant la muqueuse gastrique sont des immunoglobulines sécrétant les cellules B [64].
Ces cellules B matures dans la muqueuse gastrique produisent une réponse immunitaire locale (production des anticorps) qui est premièrement une réaction immunitaire à IgA et IgG [112].
Les anticorps n’éliminent pas la colonisation de la muqueuse gastrique ni ne préviennent la ré-infection après éradication, il n’y a donc pas d’immunité acquise [74].
Helicobacter pylori et pathologie inflammatoire:
Gastrite aigue : [67, 110,118]
Au début de l’infection, H.pylori va provoquer une gastrite antrale aiguë, généralement asymptomatique et non biopsiée mais qui peut devenir généralisée. Des changements dans la sécrétion de l’acide ou même une entéropathie avec perte des protéines peuvent se manifester.
La gastrite aiguë se manifeste par des brûlures d’estomac et des douleurs dans le haut de l’abdomen. Ces symptômes sont souvent plus intenses après les repas. Certaines personnes ont des nausées et perdent l’appétit. Il arrive parfois que la muqueuse de l’estomac, très irritée, saigne facilement et provoque une hémorragie digestive. On peut alors vomir occasionnellement du sang ou avoir des selles très foncées.
Gastrite chronique [8]:
La gastrite de type B (par opposition à la gastrite fundique A de l’ancienne classification) causée par H. pylori est une gastrite chronique mais avec présence habituelle de polynucléaires dans le chorion ; on parle alors de gastrite active.
La gastrite chronique s’accompagne parfois de brûlures ou de douleurs à l’estomac, mais elle peut se développer longtemps sans autre signe qu’une légère perte d’appétit. Il arrive qu’une hémorragie minuscule, mais régulière et persistante, entraîne une anémie par manque de fer (anémie ferriprive). Dans ce cas, la personne a le teint pâle, peut se sentir faible et éprouver parfois de la difficulté à respirer. Autrement, les symptômes sont souvent les mêmes que ceux de la gastrite aiguë.
Helicobacter pylori et pathologie ulcéreuse:
Dyspepsie non ulcéreuse :
Le terme dyspepsie décrit une digestion difficile quelle qu’en soit la cause.
Actuellement, on réserve ce terme aux troubles fonctionnels en l’absence de lésion organique décelable. D’étiologie diverse, la dyspepsie peut avoir comme origine plusieurs organes tels que l’estomac, la vésicule biliaire, le cœur, le pancréas ou les intestins.
La dyspepsie non ulcéreuse est celle dont l’origine ulcéreuse a été exclue par endoscopie. Elle s’accompagne parfois de reflux gastro-oesophagien.
L’association entre l’infection à H. pylori et la dyspepsie non ulcéreuse a été décrite dans la littérature, notamment en association avec le reflux gastro-oesophagien [135].
Cette relation a été décrite comme complexe et non encore bien élucidée, à cause probablement de la multiplicité des facteurs en jeu parmi lesquels on peut citer : [119]
Le manque de précision dans la sélection des patients. En effet dans la plupart des études, l’âge des sujets dyspeptiques était nettement supérieur à l’âge des volontaires asymptomatiques, or la prévalence de H.pylori augmente avec l’âge .De même les origines ethniques et géographique tout comme les différences de niveau socioéconomique influe sur la prévalence de l’infection à H.pylori [22].
Le caractère cosmopolite de l’expression symptomatique de la dyspepsie qui recouvre des mécanismes physiopathologiques complexes indépendant de l’infection par H.pylori [22].
Ulcère duodénale et gastrique :
Les ulcères gastroduodénaux sont de douloureuses plaies ouvertes qui se forment sur la paroi interne de l’intestin grêle ou de l’œsophage. Selon leur emplacement, les ulcères gastroduodénaux portent différents noms. S’ils se développent dans l’estomac, il s’agit d’ulcères gastriques. S’ils se retrouvent dans le duodénum (la partie supérieure des intestins) il s’agit d’ulcères duodénaux.
Un ulcère commence à se former lorsque la bactérie fragilise la muqueuse de l’estomac ou de l’intestin grêle supérieur.
Deux mécanisme pourraient intervenir : un mécanisme direct d’agression de la muqueuse faisant intervenir les propriétés cytotoxiques de la bactérie et son effet promoteur sur les médiateurs de l’inflammation, et une action indirecte d’augmentation de la sécrétion gastrique acide par le biais d’une dysrégulation des mécanismes neuro-hormonaux. Cette agression entraîne une cascade d’événements: remplacement de l’épithélium intestinal de la muqueuse duodénale par un épithélium de type gastrique (métaplasie gastrique), colonisation secondaire par H.pylori, développement d’une inflammation, d’érosions, et enfin d’ulcère [79].
Helicobacter pylori et pathologie tumorale:
Lymphome de l’estomac (Figure.5) :
Le terme de lymphome évoque en premier lieu une pathologie ganglionnaire. 25% des lymphomes surviennent en dehors des ganglions ce sont des Lymphomes extra-ganglionnaires [26].
L’estomac, est dépourvu de tissu lymphoïde à l’état normal et qui est le siège le plus fréquent des lymphomes extra-ganglionnaires, toutes les études montrent le rôle de Helicobacter pylori comme facteur déclenchant.
L’infection à H. pylori est responsable d’une gastrite chronique active au cours de laquelle vont apparaître des follicules lymphoïdes à centre clair, qui sont absents dans l’estomac normal et qui déterminent une gastrite folliculaire.
Leur présence semble pathognomonique de l’infection à H. pylori et ils sont notés dans un peu moins de la moitié des cas quand il s’agit de biopsies standards et dans 100 % des gastrites chroniques à H. pylori quand les prélèvements sont nombreux et de grande taille. Cette hyperplasie folliculaire gastrique due à H.pylori est également observée chez l’enfant. Ces follicules lymphoïdes apparaîtraient après une stimulation antigénique exercée par H. pylori sur la muqueuse gastrique. Cette hypothèse est étayée par des études in vitro montrant que les lymphocytes T sensibilisés à H. pylori fabriquent des cytokines qui stimulent la prolifération lymphoïde B (follicules), cette stimulation étant stoppée quand on supprime les H. pylori. De plus, in vivo, l’éradication de H. pylori est la première étape de tout traitement car elle permet une régression de la tumeur dans environ 60 à 80 % des cas [57,120].
L’infection à H. pylori est donc responsable de l’apparition, dans l’estomac, d’un lymphome de la zone marginale gastrique plus communément appelé lymphome gastrique du « MALT » (=mucosa-associated lymphoid tissue ) [26, 144].
|
Table des matières
HISTORIQUE
LA PREMIERE PARTIE : RAPPELS BIBLIOGRAPHIQUES
CHAPITRE I : GENERALITES
I-1-Classification
I-2- Taxonomie
I-3- Morphologie et structure de Helicobacter pylori
I-3-1-La morphologie de Helicobacter pylori
I-3-2-La structure chimique de Helicobacter pylori
I-3-2-1-La structure protéique
I-3-2-2-La structure de la paroi cellulaire
I-3-2-3-Le génome
I-4- Biologie de Helicobacter pylori
I-4-1- Ecologie
I-4-2- le PH
I-4-3- Les conditions respiratoires
I-4-4- Les conditions de température
I-4-5- Le mode nutritionnel
I-4-6- La mobilité de Helicobacter pyloi
I-5- Pathogénie de Helicobacter pylori
I-5-1-les facteurs de colonisation de Helicobacter pylori
I-5-2-Les facteurs de pathogénicité de Helicobacter pylori
I-5- 2-2- La proteine HP-NAP
I-5- 2-3- La proteine Cag A
I-6- Les réactions immunitaires et locales que provoque Helicobacter pylori
I-6-1- Induction de l’inflammation
I-6-2- La réponse immunitaire générale
I-6-3- Perturbation de la régulation de la sécrétion gastrique
CHAPITRE II : HISTOIRE NATURELLE DE L’INFECTION
II-1- Pathologies liées à l’infection à Helicobacter pylori
II-1-1- Helicobacter pylori et pathologie inflammatoire
II-1-1-1- Gastrite aigue
II-1-1-2- Gastrite chronique
II-1-2- Helicobacter pylori et pathologie ulcéreuse
II-1-2-1-dyspepsie non ulcéreuse
II-1-2-2-Ulcère duodénal et gastrique
II-1-3- Helicobacter pylori et pathologie tumorale
II-1-3-1-Lymphome de l’estomac
II-1-3-2-Le cancer gastrique ou adénocarcinome
CHAPITRE III : METHODES DE DIAGNOSTIQUE DE HELICOBACTER- PYLORI
III-1-Les tests non invasifs
III-1-1-Le diagnostique sérologique
a- Les avantages de la sérologie
c- Les méthodes utilisées
1- Méthode ELISA
2-WESTERN-BLOT
III-1-2-Le test respiratoire à l’urée marquée ou < urea breath test C. 13 >
a- Les avantages du test respiratoire à l’urée
b- La méthode
III-1-3- Détection des antigènes dans les selles ou HpSA
III-2- Les tests invasifs
III-2-1- Endoscopie et biopsie
III-2-2- Le test rapide à l’urée
a- Les avantages du test
b- La limite du test
c- La méthode
III-2-3- L’amplification génique ou la PCR
a- Les avantages du test
b- Les limites de ce test
c- La méthode
III-2-4- Examen direct
a- Au laboratoire de bactériologie
La mise en culture
Identification
b- Au laboratoire d’anatomopathologie
III-3- Antibiogramme
CHAPITRE IV : TRAITEMENT DE L’INFECTION A Helicobacter pylori
IV-1- Traitement de première ligne
IV-1-1- Facteurs d’échec du traitement
IV-1-1-1- La mauvaise application de la trithérapie
IV-1-1-2- La résistance bactérienne
IV-1-2- Adaptation du traitement de la première ligne à l’antibiogramme
IV-1–3- Contrôle de l’éradication
IV-3-Le traitement du troisième ligne
DEUXIEME PARTIES : EPIDEMIOLOGIE
I- Réservoir de Helicobacter pylori
I-1- Réservoir humain
I-2- Réservoir animal
I-3- Réservoir environnemental
II- Mode de transmission
II-1 Transmission interhumaine
II-1-1- Transmission par voie orale- orale
II-1-2- Transmission par voie féco-orale
II-1-3- Transmission par le matériel d’endoscopie
III- La prévalence de l’infection à Helicobacter pylori
III-1- Dans les pays développés
III-2- Dans les pays en voie de développement
IV- Les habitudes de vie et infection à Helicobacter pylori
IV-1- Tabac
IV-2- Alcool
IV-3- Prise des médicaments
IV-4- Le jus de canneberge
IV-5- Stress oxydant : une réaction de défense mutagène
IV-6- Effet du chocolat
TROISIEME PARTIE : TRAVAIL PERSONNEL
I- Cadre d’étude
I-2- Les infrastructures sanitaires
I-3- Présentation du service de Gastro-entérologie de l’hôpital IBN ROCHD
II- Buts du travail
III- Matériel d’étude
IV- Méthodes
IV-1- Prélèvement
IV-2- Réalisation du Clo-test*
IV-3-Bactériologie
IV-4-Anatomopathologie
V- RESULTATS
V-1- PREVALENCE DE HELICOBACTER PYLORI
V-2- PROFIL EPIDEMIOLOGIQUE
V-2-1- Répartition suivant l’âge
V-2-2- Répartition suivant le sexe
V-2-3- Répartition suivant le niveau socioéconomique
VI- DISCUSION
VI-1- Helicobacter pylori et sexe
VI-2- Helicobacter pylori et âge
VI-3- Helicobacter pylori et niveau socioéconomique
VI-4 -Helicobacter pylori et ulcère duodénal
RECOMMANDATIONS
CONCLUSION
RESUME
BIBLIOGRAPHIE
Télécharger le rapport complet