Généralité sur l’eau et sa Pollution
Généralité sur l’eau
L’eau peut se trouver sous la forme liquide, solide, ou vapeur. Elle peut être chargée de sels minéraux, de matières organiques, de bactéries en plus ou moins grande quantité selon le lieu où elle se trouve. C’est pourquoi l’eau est un milieu hétérogène, relativement peu pur et dont la composition est fonction de la nature des terrains géologiques traversés. L’eau contient des substances ou des microorganismes qui par leurs natures et leurs concentrations peuvent être, acceptables, indésirables, voir toxiques ou dangereux. L’eau prélevée dans le milieu naturel n’est généralement pas utilisable directement, elle doit subir des traitements pour être consommée sans danger par l’ensemble de la population. [5]
Les eaux souterraines
Les eaux souterraines proviennent des pluies pour une faible part. Cependant, la proportion la plus notable retourne dans l’atmosphère par évaporation et qu’une autre fraction rejoint les océans par les fleuves et les rivières. Ce processus s’arrête lorsqu’elle atteint une couche imperméable. Historiquement, les eaux souterraines ont toujours été une source d’eau de haute qualité pour l’alimentation, par opposition aux eaux de surface, polluées par les activités humaines (agricoles, industrielles, ou autres). Normalement l’eau souterraine est débarrassée des organismes qui sont retenus ou adsorbés à travers des terrains perméables qui laisse libre cours à toutes sortes de processus physico-chimiques tels que échange d’ions, adsorption, précipitation, transformation chimiques, biodégradation. C’est la raison pour la quelle l’eau souterraine diffère de l’eau de surface à la fois sur le plan chimique que biologique. Elle peut atteindre également une qualité microbiologique acceptable, selon l’épaisseur du sol, sa texture, sa structure et son activité biologique. Ainsi, les eaux souterraines sont beaucoup moins coûteuses comparativement aux eaux de surface exigeant des traitements de plus en plus complexe. Enfin, comparativement, les gisements des eaux souterraines sont beaucoup plus importants que ceux des eaux de surface [6].
Les eaux de surfaces
Les eaux de surface proviennent surtout des pluies et sont parfois constituées d’un mélange d’eaux de ruissellement et d’eaux souterraines. Leur captage se fait :
• par des citernes ou des aires de captage, pour l’eau de pluie.
• par des prises, pour les étangs et réservoirs ;
• par des barrages et prises, pour les cours d’eau.
Les eaux de surface peuvent parfois être utilisées à l’état naturel comme eau de boisson. Pour éviter les contaminations, elles sont toujours traitées au préalable [6].
Les paramètres de l’eau
Les paramètres organoleptiques de l’eau
Il s’agit de la saveur, de la couleur, de l’odeur et de la transparence de l’eau. Si ces paramètres n’ont pas de signification sanitaire, par leur dégradation, ils peuvent indiquer un certain degré de pollution, un mauvais fonctionnement des installations de traitement ou de distribution. Ils permettent donc au consommateur de porter un jugement sur la qualité de l’eau. Ils comprennent ainsi :
• La couleur qui peut être due à la présence de matières organiques colorées (substances humiques, d’élément métalliques provenant de la dissolution des roches, tels que le manganèse (noir), le cuivre (bleu), le fer (rouge) et de particules colloïdales en suspension. La couleur peut aussi avoir une origine biologique par exemple l’eutrophisation engendrée par la pollution d’algues ou la présence de bactéries qui colorent l’eau en vert ou en rouge. Les colorants chimiques, les phénols et leurs dérivés, les pigments, dans l’eau, confèrent à celle-ci leur coloration caractéristique. [7]
• L’odeur qui a pour origine principalement la présence de composés organiques volatils ou de gaz. Les odeurs peuvent révéler la présence de la terre, de moisissures, d’herbes pourries, de fosses sceptiques et même des micro-organismes dont les métabolismes sont odorants, [7]
• Le goût qui peut être défini comme étant l’ensemble des sensations gustatives, olfactives et de sensibilité chimique perçue lorsque l’aliment ou la boisson est dans la bouche.
• La saveur qui peut être définie comme étant l’ensemble de sensations perçues à la suite de la stimulation, par certaines substances solubles des bourgeons gustatifs. Il existe en général quatre saveurs élémentaires : Saveur acide, saveur sucrée, saveur amère saveur salée. [8].
Généralité sur la pollution de l’eau
La pollution de l’eau est due très souvent aux activités humaines ainsi qu’aux phénomènes naturels. Elle a des effets multiples qui touchent aussi bien la santé publique que les organismes aquatiques .
Les différents types de pollution de l’eau
La pollution de l’eau est l’ensemble des nuisances auxquelles peut être exposé son usager. La pollution engendrée peut être d’ordre physique (radioactivité, élévation de la température…), chimique (rejets agricoles, industriels et urbains) et microbiologique (rejets urbains, élevage…). Pour mieux évaluer la pollution, il existe des paramètres qui permettent d’estimer l’ampleur de celle-ci en fonction de ses caractéristiques.
La pollution physique de l’eau
On parle de pollution physique lorsque le milieu marin est modifié dans sa structure physique par divers facteurs :
• un rejet d’eau douce qui fera baisser la salinité d’un lieu,
• un rejet d’eau réchauffée ou refroidie (par une centrale électrique ou une usine de regazéification de gaz liquide),
• un rejet de liquide ou solide de substance modifiant la turbidité du milieu (boue, limon, …), d’une source de radioactivités …
La plupart du temps, un rejet n’est jamais une source unique et les différents types de pollution sont mélangés et agissent les uns sur les autres. Ainsi, un égout rejette des déchets organiques, des détergents dont certains s’accompagnent de métaux lourds (pollution chimique), des micro-organismes (pollution biologique), le tout dans de l’eau douce (pollution physique) [8].
|
Table des matières
INTRODUCTION
PREMIERE PARTIE : ETUDES BIBLIOGRAPHIQUES
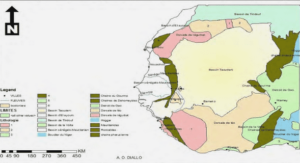
I- PRESENTATION DE LA ZONE D’ETUDE
I-1.Région du Brakna
I-2-Le lac d’Aleg
II- Généralité sur l’eau et sa pollution
II.1- Généralité sur l’eau
II.1.1- Les eaux souterraines
II.1.2.Les eaux de surfaces
II.1.3- Les paramètres de l’eau
II.1.3.1- Les paramètres organoleptiques de l’eau
II.1.3.2- Les paramètres physiques de l’eau
II.1.3.3- Les paramètres chimiques de l’eau
II.1.4- La caractérisation physico-chimiques des eaux
II.1.5 – Notion de norme
II.2- Généralité sur la pollution de l’eau
II.2.1- Les différents types de pollution de l’eau
II.2.1.a- La pollution physique de l’eau
II.2.1.b- La pollution chimie de l’eau
II.2.1.c- La pollution microbiologique de l’eau
II.2.2-Effet de la pollution sur la santé
DEUXIEME PARTIE : ETUDE EXPRIMENTALES
I- PRELEVEMENTS DE LES ECHANTILLONS ET ANALYSESPHYSICOCHIMIQUES
I.1- Le choix du circuit et les stations de prélèvement
I.2- Echantillonnage et Méthodes d’analyses
I.3-Protocole d’Analyses physico-chimiques
I.3.1.- Mesure du pH
I.3.2- -Mesure de la Température
I.3.3- -Mesure de la Conductivité électrique (C.E)
I.3.4- -Mesure de Sels totaux dissous (TDS)
I.3.5- – Mesure de la Turbidité
I.3.6- Mesure volumétriques
I.3.6.a- Dosage de Titre hydrotimétrique
I.3.6.b- Dosage simultané du calcium et du magnésium
I.3.6.c- Dosage de chlorure
I.3.7- Mesure par spectrophotométrie UV Visible hmed DICK
I.3.7.a- Dosage de nitrates
I.3.7.b- Dosage de nitrites
I.3.7.c- Dosage d’ammonium
I.3.7.d- Dosage de sulfate
I.3.8- Mesure par photomètre à flamme
TROISIEME PARTIE : RESULTATS ET INTERPRTATIONS
I-RESULTATS PHYSICO-CHIMIQUES
II- INTERPRETATION DES RESULTATS
II.1- Les paramètres physiques
II.1.1 Le Potentielle d’Hydrogène (pH)
II.1.2 Température
II.1.3 La Conductivité électrique
II.1.4 Les Sels totaux dissous (TDS)
II.1.5 La Turbidité
II.2- Les paramètres chimiques
II.2.1- Titre hydrotimétrique
II.2.2- Calcium
II-2-3- Magnésium
II.2.4- Chlorure
II.2.5- Sodium
II-2.6-Potassium
II.2.7- Nitrate
II-2.8-Nitrite
II-2.9 -Ammonium
II.2.10- Sulfate
CONCLUSION
REFERENCES BIBLIOGRAPHIQUES