Télécharger le fichier pdf d’un mémoire de fin d’études
DEMARCHE DIAGNOSTIQUE DEVANT L’INSUFFISANCE RENALE CHRONIQUE
Selon la Haute Autorité de Santé française, dans le guide de parcours de soins de la maladie rénale chronique, 3 grandes étapes de démarches sont recommandés :
Dépistage
Faire le diagnostic de la MRC
Faire une évaluation initiale de la MRC
Dépistage
Le dépistage consiste à :
Identifier les patients à risque de maladie rénale chronique, qui se fera en médecine ambulatoire, recherchant :
• Diabète
• Hypertension artérielle traitée ou non
• Age > 60 ans
• Obésité (IMC > 30 kg/m²)
• Maladie cardio-vasculaire athéromateuse
• Insuffisance cardiaque
• Maladie de système ou auto-immune (lupus, vascularite, polyarthrite rhumatoïde…)
• Affection urologique (uropathie obstructive, infections urinaires récidivantes…)
• Antécédents familiaux de maladie rénale ayant évolué au stade d’insuffisance rénale chronique
• Exposition à des toxiques professionnels (plomb, cadmium, mercure, solvants organiques)
• Traitement néphrotoxique antérieur (AINS au long cours, chimiothérapie, radiothérapie…)
Rechercher les marqueurs d’atteinte rénale (protéinurie, hématurie, leucocyturie) que se feront en médecine du travail, à partir du test de bandelettes urinaires sur échantillon d’urines.
Le dépistage est réalisé une fois par an et porte sur :
• l’estimation du débit de filtration glomérulaire (DFG estimé), réalisée à partir du dosage de la créatininémie
• la mesure de l’albuminurie1 réalisée à partir d’un échantillon urinaire à tout moment de la journée, et dont le résultat est exprimé sous la forme d’un ratio albuminurie/créatininurie (A/C).
Diagnostic de la MRC
Deux cas peuvent se présenter :
Si le dépistage est positif lors du suivi de patient à risque, le diagnostic est confirmé par le médecin généraliste en répétant les tests du dépistage :
• par la persistance d’une diminution du DFG (DFG < 60m l/min/1,73 m²) sur deux ou trois examens consécutifs positifs réalisés dans les trois mois et avec la même technique de dosage de la créatininémie ;
• ou par la persistance d’une albuminurie sur deux ou trois examens consécutifs positifs réalisés dans les 3 mois.
Si des signes d’atteintes rénales sont présents :
• Une situation nécessitant une prise en charge spécialisée sera à identifier :
immédiate : glomérulonéphrite rapidement progressive (dégradation rapide de la fonction rénale : syndrome glomérulaire, signes extra-rénaux), insuffisance rénale aiguë (obstacle,toxique, insuffisance rénale fonctionnelle, etc.) ;
ou rapide : calcul, hydronéphrose, tumeur, hypertension artérielle réfractaire, syndrome néphrotique, oedèmes, hématurie, signes extra-rénaux et généraux …
• En dehors de ces situations, l’affirmation du caractère chronique de la maladie rénale est établie lorsque l’un des signes d’atteinte rénale persiste pendant plus de 3 mois :
Diminution du DFG : DFG < 60ml/min/1,73 m² ;
o Protéinurie ou albuminurie ;
o Hématurie : GR > 10/mm3 ou 10 000/ml (après avoir éliminé une cause urologique) ;
o Leucocyturie : GB >10/mm3 ou 10 000/ml (en l’absence d’infection)
o Anomalie morphologique à l’échographie rénale : asymétrie de taille, contours bosselés, reins de petite tailles ou gros reins polykystiques, néphrocalcinose, kyste.
Evaluation de la maladie rénale chronique
Orienter le diagnostic étiologique
Les éléments d’orientation diagnostique sont donnés par l’interrogatoire, l’examen clinique et les examens paracliniques.
Interrogatoire et examen clinique
• Recherche des antécédents : atteinte rénale et ou urinaire, maladie cardio vasculaire, diabète, facteurs de risque cardio-vasculaire, tabagisme, antécédents familiaux de maladie rénale ;
• Recherche d’une exposition a des produits néphrotoxique : professionnelle (plomb, mercure, cadmium, solvants organiques), médicamenteuse (médicament néphrotoxique ou médicament a risque d’accumulation liée a la MRC avec risque d’EIs), alimentaire (phytothérapie herbes chinoises) et produits de contraste ;
• Mesures : poids, taille (IMC), tour de taille, pression artérielle (réaliser une MAPA en cas de doute sur le diagnostic d’HTA, et sensibiliser le patient a l’intérêt de l’automesure pour son suivi tensionnel)
• Auscultation cardiaque, recherche de souffle vasculaire, pouls périphériques
• Recherche d’œdèmes, appréciation de l’état d’hydratation, reins palpables, signes cliniques extra-rénaux de maladie systémique, obstacle urologique (troubles de la miction, globe vésical, touchers pelviens)
Examens complémentaires systématiques
• Echographie rénale
• Créatininémie et DFG estime : évaluation du stade et de l’évolutivité de la MRC
• Albuminurie, hématurie, leucocyturie, cytologie urinaire quantitative :
évaluation de l’évolutivité de la MRC, diagnostic d’une néphropathie glomérulaire évolutive
• Exploration anomalies lipidiques : recherche de facteur de risque cardio-vasculaire
• Glycémie a jeun (chez non-diabétique) : recherche de facteur de risque cardio vasculaire
• Uricémie : valeur initiale
• 25-OH-Vit D (ne pas doser la 1,25OH vit D) : valeur initiale, dépistage d’une carence
• Hémogramme : valeur initiale, surveillance ultérieure de l’anémie
• Na+, K+, chlore, bicarbonates Troubles hydro-électrolytiques
Examens complémentaires non systématiques
• Echographie vésicale : recherche étiologique, anomalies du bas appareil, d’un trouble de la vidange vésicale, d’un résidu post mictionnel
• Urée et sodium sur les urines 24 h : à partir stade 3B, évaluation des apports alimentaires
• Albuminémie, urée sanguine : systématique à partir stade 3B, valeur initiale pour la surveillance ultérieure de dénutrition
• Parathormone, Ca2+, phosphore : systématique à partir stade 3, troubles phosphocalcique
Évaluer le stade de la maladie rénale chronique
Le stade de maladie rénale chronique est défini à partir du DFG estimé et de la présence de marqueurs d’atteinte rénale (tableau I). Le stade 3 d’insuffisance rénale modérée intègre deux niveaux de sévérité (stade 3A et 3B).
Évaluer la progressivité de la maladie rénale chronique
La maladie rénale chronique est considérée comme évolutive, c’est-à-dire à risque de progression vers l’IRCT, dans les situations suivantes :
• Déclin annuel rapide du DFG
Le déclin annuel est calculé de la manière suivante : DFG année n – DFG année n+1 et évalué avec les repères suivants :
déclin annuel « physiologique » observé après 40 ans : < 2 ml/min/1,73 m²/an,
déclin annuel « modéré » : ≥ 2 et < 5 ml/min/1,73 m²/an,
déclin annuel « rapide » : ≥ 5 ml/min/1,73 m²/an ;
• Présence d’albuminurie : le risque d’évolution vers le stade d’IRCT n’est pas seulement fonction du DFG mais aussi de la présence et de l’importance de l’albuminurie;
Anémie au cours d’une insuffisance rénale chronique
Définition de l’anémie au cours de l’insuffisance rénale chronique
L’anémie se définit classiquement selon les critères de l’Organisation mondiale de la santé (OMS) de 1968 avec une hémoglobinémie inférieure 12 et 13 g/dl chez la femme et l’homme respectivement.
Toutefois, cette définition a été remise en question au cours des années par différentes publications. En effet, les EuropeanRenal Best Practice Guidelines(ERBP) ont proposé en 2004 de poser le diagnostic de l’anémie pour une hémoglobinémie inférieure à 13,5 et 11,5 g/dl chez l’hommeet chez la femme, respectivement, ainsi que pour une hémoglobinémie inférieure à 12 g/dl pour les plus de 70 ans [16].
En 2012, KDIGO a recommandé que le seuil de l’anémie chez un patient insuffisant rénal soit à partir de l’hémoglobine inférieure à 13 g/dl et 12 g/dl respectivement chez l’homme et chez la femme.
Physiopathologie
L’anémie chez les patients avec une insuffisance rénale chronique(IRC) peut prendre plusieurs origines. Elle est dite multifactorielle, due à un déficit en EPO, à une inhibition de l’érythropoïèse induite par l’urémie, à une diminution de la durée de vie des globules rouges et à un déséquilibre de l’homéostasie du fer [17].
Anomalie de l’érythropoïétine
L’EPO est une glycoprotéine produite au niveau des cellules interstitielles péri-tubulaires rénales, en réponse à l’hypoxie tissulaire. Une chute de la pO2 tissulaire rénale stimule la production d’EPO afin d’augmenter la masse érythrocytaire et ainsi la capacité de transport de l’oxygène.
L’hypothèse physiopathologique actuelle explique la diminution de la synthèse de l’EPO dans l’insuffisance rénale par l’installation progressive d’une fibrose interstitielle et une apoptose des cellules myofibroblastiques à l’origine de la synthèse de l’EPO d’ une part et par l’inhibition de son action induite par les toxines urémiques d’ autre part. Dans ce cas, l’anémie est dite d’origine « rénale ».Le déclin du débit de filtration glomérulaire corrèle vraisemblablement à celui de la synthèse d’EPO [18].
Déséquilibre de l’homéostasie du fer
Les patients en hémodialyse, et de manière plus générale les patients insuffisants rénaux, ont fréquemment un déficit martial réel dû à 3 mécanismes :
• Pertes sanguines au niveau des circuits d’hémodialyse, par de nombreuses prises de sang et de fréquentes procédures chirurgicales auxquelles ils sont soumis (par exemple mise en place d’abords vasculaires).
• Perturbation de l’absorption intestinale de fer par plusieurs traitements souvent administrés en cas d’insuffisance rénale (inhibiteurs de la pompe à protons, chélateurs du phosphate…) [19].
• Diminution de l’absorption intestinale de fer due à une élévation du taux plasmatique de l’ hepcidine.
En effet, l’ hepcidine qui est une protéine essentiellement produite par le foie, particulièrement élevée en cas d’insuffisance rénale, est actuellement identifiée comme un facteur important contribuant à la diminution de l’absorption de fer intestinal. C’est le principal peptide régulateur du métabolisme du fer. En induisant la dégradation de la ferroportine, elle empêche la sortie du fer des entérocytes duodénaux ainsi que sa libération par le système réticuloendothélial (cellules de Kupffer et macrophages spléniques, entre autres), diminuant ainsi sa disponibilité plasmatique. Les stocks de fer restent ainsi piégés au niveau du système réticuloendothélial et ne peuvent pas être utilisés pour l’érythropoïèse [17].
Les principaux régulateurs de la production d’hepcidine sont l’état inflammatoire, le fer et l’insuffisance rénale qui en augmentent le taux, tandis que l’anémie, l’hypoxie et l’EPO ont tendance à en réduire la production [20] .Chez les patients insuffisants rénaux ou en dialyse, on retrouve des taux élevés d’hepcidine en raison de cette balance où les facteurs stimulateurs sont prédominants [21 ,22].
Autres mécanismes
Anomalie de l’érythropoïétine, troubles de l’homéostasie du fer sont les 2 principales causes de l’anémie au cours de l’insuffisance rénale chroniques. D’autres facteurs peuvent également y contribuer : diminution de la durée de vie de globules rouges, hémoglobinopathie, carences en folate ou en vitamine B12, états inflammatoires, hyperparathyroïdie grave, intoxication par l’aluminium.
|
Table des matières
INTRODUCTION
PREMIERE PARTIE : RAPPELS
I. GENERALITE SUR L’INSUFFISANCE RENALE CHRONIQUE
I.1. Définition
I.2. Epidémiologie.
I.3. Physiopathologie de l’insuffisance rénale chronique.
I.3.1. Caractéristiques de l’insuffisance rénale chronique
I.3.1.1.Critère de destruction néphronique.
I.3.1.2. Substratum anatomique de l’insuffisance rénale chronique
I.3.1.3. Réponse adaptative rénale.
I.3.1.4. Répercussions de l’insuffisance rénale chronique sur l’homéostasie
II. DEMARCHE DIAGNOSTIQUE DEVANT L’INSUFFISANCE RENALE CHRONIQUE.
II.1. Dépistage.
II.2. Diagnostic de la maladie rénale chronique.
II.3. Evaluation de la maladie rénale chronique .
II.3.1. Orienter le diagnostic étiologique.
II.3.2. Évaluer le stade de la maladie rénale chronique.
II.3.3. Évaluer la progressivité de la maladie rénale chronique.
III. ANEMIE AU COURS D’UNE INSUFFISANCE RENALE CHRONIQUE
III.1. Définition de l’anémie au cours de l’insuffisance rénale chronique
III.2. Physiopathologie.
III.2.1. Anomalie de l’érythropoïétine.
III.2.2. Déséquilibre de l’homéostasie du fer.
III.2.3. Autre mécanismes.
III.2.4. Facteurs associés à l’anémie chez lespatients atteints d’insuffisancerénale chronique
III.2.5. Caractère de l’anémie au décours d’une insuffisance rénale chronique
III.3. Prise en charge de l’anémie au cours d’une insuffisance rénale chronique
III.3.1. Dépistage
III.3.2.Examens complémentaires initiaux recommandés au cours d’une anémie au cours de l’insuffisance rénale chronique
III.3.3. Bilan martial.
III.3.4. Traitement martial.
III.3.5. Traitement par érythropoïétine.
III.3.6. Transfusion.
DEUXIEME PARTIE : METHODES ET RESULTATS
I. MATERIELS ET METHODES.
II. RESULTATS.
II.1. Résultats généraux.
II.2. Répartition de la population selon les variables de l’étude
II.2.1. Selon l’âge.
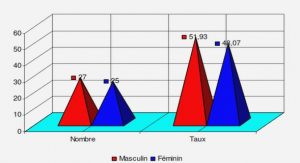
II.2.2. Selon le genre.
II.2.3. Selon la profession.
II.2.4. Selon les revenus salariaux mensuels.
II.2.5. Selon le lieu où habitent les patients.
II.2.6. Selon le mode de déplacement.
II.2.7. Selon les signes cliniques.
II.2.8. Selon les antécédents des patients.
II.2.9. Selon les étiologies de la maladie rénale chronique.
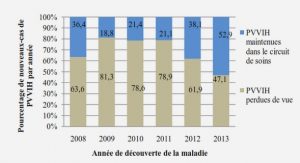
II.2.10. Selon les étiologies de l’anémie.
II.2.11. Selon le taux de l’hémoglobine.
II.2.12. Selon la créatininémie avec le débitde filtration glomérulaire
II.2.13. Selon le traitement de l’anémie.
II.2.14. Selon la durée d’hospitalisation.
II.3. Evaluation de coût global des examens paracliniques.
II.3.1. Pour le dépistage.
II.3.1.1. Par rapport au SMIG.
II.3.1.2. Par rapport au revenu salarial des patients.
II.3.2. Pour la recherche étiologique de l’anémie.
II.3.2.1. Par rapport au SMIG.
II.3.2.2. Par rapport au revenu salarial des patients.
II.3.3. Pour le traitement.
II.3.3.1. Coût de consommable au prélèvement pour les examens paracliniques nécessaires
II.3.3.1.1. Par rapport au SMIG.
II.3.3.1.2. Par rapport au revenu salarial des patients
II.3.3.2. Evaluation de coût global de traitement de l’anémie au cours de IRC
II.3.3.2.1. Pour l’anémie non classée.
II.3.3.2.2. Pour l’anémie classée.
TROISIEME PARTIE : DISCUSSION
I. Aspects épidémio-cliniques des malades insuffisants rénaux chroniques anémiques.
I.1. Selon l’âge.
I.2. Selon le genre.
I.3. Selon la profession.
I.4. Selon le revenu salarial.
I.5. Selon le lieu de domicile.
I.6. Selon le mode de déplacement.
I.7. Selon les signes cliniques.
I.8. Selon les antécédents.
II. Aspect étiologique.
II.1. Selon les étiologies des maladies rénales chroniques.
II.2. Selon les étiologies de l’anémie.
III. Aspect paraclinique.
III.1. Selon le taux de l’hémoglobine.
III.2. Selon la créatininémie avec le débit de filtration glomérulaire.
IV. Aspect thérapeutique.
V. Aspect sur le coût de traitement de l’anémie au cours de la maladie rénale chronique.
V.1. Coût direct.
V.1.1. Pour le dépistage.
V.1.2. Pour la recherche étiologique.
V.1.3. Pour les consommables au prélèvement pour examens paracliniques.
V.1.4. Pour le traitement proprement dit.
V.2. Coût indirect.
CONCLUSION.
REFERENCES BIBLIOGRAPHIQUES
ANNEXE
Télécharger le rapport complet